作为新一代的高选择性及高亲和力5-羟色胺4(5-HT4)受体激动剂,普芦卡必利(力洛®)自2009年在欧盟上市以来,从实质上改善了慢性便秘(CC)患者的治疗效果,带来了明显获益。普芦卡必利通过特异性、选择性地刺激肠道5-HT4受体,刺激肠道产生高幅推进性收缩,促进肠道(特别是结肠)的蠕动,在提升肠道动力和重塑排便功能方面有显著作用。大量循证证据已充分证实,普芦卡必利治疗CC有效,可提升肠道动力、重塑排便功能,并已得到众多国内外指南推荐,成为了CC患者新的治疗选择。目前,普芦卡必利已在30个国家和地区上市,用于治疗成年女性患者中通过轻泻剂难以充分缓解的CC症状,在新加坡、澳大利亚等国家同时获批用于男性CC患者。2013年,普芦卡必利在中国上市,为我国的CC患者带来了新的治疗选择。
2008-2009
欧美三项关键Ⅲ期研究
多中心、随机、安慰剂对照Ⅲ期USA-11、INT-6和USA-13研究结果一致证实,普芦卡必利治疗欧美CC患者安全有效。三项关键研究在2008-2009年间,分别发表于《新英格兰医学杂志》(N Engl J Med)、《消化道》(Gut)和《消化药理学和治疗学》(Aliment Pharmacol Ther)。
结果显示,12周治疗结束后,USA-11、INT-6和USA-13研究中,每天1次普芦卡必利2 mg组和4 mg组达到每周完全自发排便(SCBM)≥3次的患者比例显著高于安慰剂组。针对这三项研究的汇总分析显示,12周治疗后,普芦卡必利(2 mg)组每周SCBM≥3次的患者比例明显高于安慰剂组(23.6%对11.3%,P≤0.001,图1)。在次要终点方面,与安慰剂组相比,普芦卡必利治疗后的每周SCBM增加≥1次及每周自发排便(SBM)增加≥1次的患者比例(图2)、排便次数、大便性状等也显示明显优势。
2010
长期随访研究
2010年,两项开放标签、长期随访临床研究(INT-10和USA-22研究)结果发表在Aliment Pharmacol Ther杂志。这两项长期随访研究纳入完成了为期12周治疗的三项关键研究(USA-11、INT-6及USA-13研究)的CC患者,给予普芦卡必利治疗24或36个月,每隔3个月用便秘评估—生活质量(PAC-QoL)进行评价1次。
结果显示,1691例患者完成为期12周的上述三项关键研究,其中1455例(86%)继续接受了普芦卡必利治疗,进入长期随访的非盲法研究。结果显示,患者的PAC-QoL评分改善≥1分的患者比例不断提高,这种改善从治疗3个月开始并可持续至第18个月,表明普芦卡必利长期治疗患者生活质量满意度持续改善。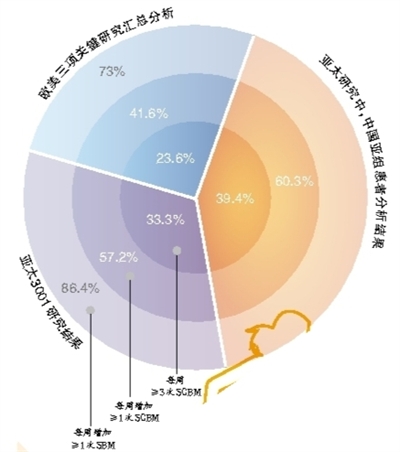
2012
亚太3001研究
2012年发表在《神经胃肠病学与动力》(Neurogastroenterol Motil)杂志的亚太多中心、随机对照Ⅲ期3001研究首次证实,普芦卡必利(2 mg qd)对亚太地区CC患者同样安全有效。
结果显示,对于501例亚太CC患者,普芦卡必利治疗后每周SCBM≥3次的患者比例显著高于安慰剂(33.3%对10.3%,P<0.001,图1)。其中,中国亚组患者的结果令人鼓舞,接受普芦卡必利的上述有效性终点达到39.4%(图2)。最初4周、随后5~8周和9~12周,普芦卡必利组每周SCBM≥3次的患者比例均明显高于安慰剂组。此外,普芦卡必利组患者每周SCBM的平均次数、排便硬度、每次排便费力程度、每周应用润肠药或灌肠的天数以及轻泻剂使用等均有明显改善。[8540601] (芳菲)
■ 普芦卡必利的发展之路
87项Ⅰ~Ⅲ期临床研究证实了普芦卡必利的疗效和安全性。
2010年
普芦卡必利在欧盟上市。
2010年
世界胃肠病组织(WGO)的《CC诊治指南》中,普芦卡必利获1A级推荐用于治疗CC患者。
2012年12月
截至2012年12月,普芦卡必利已在30个国家获批上市,其中包括欧盟、加拿大、澳大利亚以及亚洲等多个国家,其中在英国、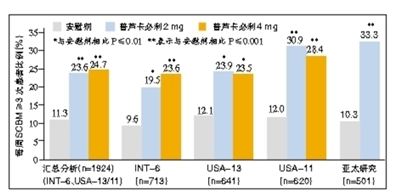 希腊、瑞士、德国等欧洲国家予以报销。
希腊、瑞士、德国等欧洲国家予以报销。
2012年12月
普芦卡必利获中国国家食品药品监督管理总局(CFDA)审批上市。
2013年
最新发布的《中国CC诊治指南》指出,研究表明普芦卡必利能缩短结肠传输时间,安全性和耐受性良好,推荐其用于CC的治疗(ⅠA级推荐)。


评论