病例简介
病史
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
现病史及家族史
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,肛门指诊未及异常。
入院检查
血常规无明显异常;血液生化检查未见明显异常; 肿瘤标志物:癌胚抗原(CEA) 69.28 ng/ml。
胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3 cm,周边黏膜不规则(图1);病理检查为腺癌。
CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。
诊断 胃癌肝转移。
MDT讨论及诊治经过
第一次MDT讨论(2010年10月)
影像科 该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。
肿瘤内科 多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu) 及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF 3 周方案。
胃肠外科 胃癌肝转移根据美国国立综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。
治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1 为转移灶局限于一个肝叶,H2 为两个肝叶可见数个散在转移灶,H3 为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。
对于原发灶能R0 切除的H1 型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2 和H3 型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。
肝脏外科 对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。
消化内科 对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。
第一次治疗经过
2010年10月 采用DCF 3 周方案 [多西他赛100 mg/m2,第1 天;顺铂20 mg,1次/日,第1~5 天;5-Fu 750 mg/m2,1次/日,第1~5天,每日持续静脉滴注6小时以上],解救化疗4 个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6 个周期。
2011年3月 复查CEA 48.26 ng/ml,CT 检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2 ×2 cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。
2011年9月 CEA升高为91.20 ng/ml,CT示肝脏转移灶增大(图4)。
2011年9月 再次组织全院胃癌MDT讨论。
第二次MDT讨论(2011年9月)
影像科 2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4 cm、1.2×1.1 cm、1.1×1.0 cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。
肿瘤内科 患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟) 等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。
针对该患者建议行人表皮生长因子受体2(HER2) 等相关检测,以决定是否需要考虑联合靶向药物治疗。
胃肠外科 胃癌肝转移手术治疗是一种姑息性治疗手段, 在没有并发症前提下手术意义不大。
针对该患者用改良DCF 方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。
肝脏外科 患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。
介入科 该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA 升高。
由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
第二次治疗经过
2011年9月 采用TOF 二线方案化疗(紫杉醇60 mg/m2,第1、8 天;奥沙利铂65 mg/m2,第1、8 天;5-Fu 750 mg/m2,1次/日,第1~5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT 提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5 cm。
2012年1月 继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。
2013年4月 定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4 cm(图5),磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA 170.48 ng/ml,行进一步治疗中。
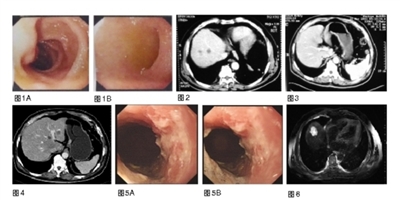
图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3 cm,周边黏膜不规则
图2 CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
图3 CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节
图4 CT(2011年9月)示肝脏转移灶再次出现
图5 胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4 cm
图6 MRI(2013年4月)示肝内多发转移结节较前增多增大
MDT治疗体会
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%~9.9%。胃癌肝转移(GCLM)不仅预后差(5年生存率<10%),而且是最常见的死亡相关原因。
对同时合并肝内及肝外转移的胃癌,治疗应遵循晚期胃癌的姑息治疗原则,而对仅伴有肝内转移的胃癌患者,有望通过转化性治疗、联合手术等局部治疗手段的综合治疗模式延长生存期。GCLM的治疗方法可归纳为以下几种方法。
GCLM的“根治性”手术 该方式意味着实施针对原发癌灶的D2胃癌切除联合肝转移灶切除。GCLM患者“根治性”手术适应证应把握下述几点:①无腹腔种植或其他肝外转移;②原发灶具备D2胃癌切除可能;③肝转移灶技术上可切除,残肝贮备有保障。
若转移灶不可切除,原发灶出现梗阻、穿孔、出血等并发症时,可实施胃癌姑息性切除手术。
新辅助化疗(NCT) 1989年NCT被应用在治疗胃癌患者中,而GCLM是美国国家综合癌症网络(NCCN)指南所推荐的NCT治疗适应证。
研究表明对于GCLM患者,若仅行根治性手术,大部分患者术后易复发,而术后化疗对延长术后生存作用有限,NCT却可显著提高GCLM患者手术切除率和术后生存。
肝转移灶的放射介入治疗 常用手段包括肝动脉灌注化疗(HAI)、肝动脉栓塞治疗(TAE)及肝动脉化学栓塞疗法(TACE)。
HAI利用化疗药的首过效应,使肝转移灶具有较高的局部药物浓度,且无明显的全身毒副反应,不仅用于控制局部转移灶,还作为术前降期治疗方案。
肝转移灶的消融治疗 常见的消融技术包括射频消融(RFA)、微波消融(MWA)和冷冻消融,每一项均可单独使用或与胃癌手术联合应用,分别可行超声或CT引导的经皮途径、经腹腔镜途径或开放手术途径。
肝转移灶的分子靶向治疗 分子靶向治疗是近年胃癌综合治疗的研究热点,目前已发现多个胃癌相关的治疗靶点(EGFR、HER2、VEGF等),针对这些靶点的分子靶向药物也开始应用于胃癌治疗。
分子靶向治疗药物主要包括具有分子靶向性的表皮生长因子受体阻断剂、单克隆抗体、针对某些癌基因和癌细胞遗传学标志的药物、抗肿瘤血管生成的药物、抗肿瘤疫苗以及基因治疗。
总结
对于胃癌肝转移,尤其应强调多学科协作在治疗中的应用,使肿瘤治疗个体化,并建议针对胃癌肝转移开展多中心协作的前瞻性随机对照临床研究,探索并规范胃癌肝转移的治疗模式,进一步改善胃癌肝转移的预后。
胃癌MDT模式是实现胃癌规范化综合治疗的有效形式,其基本人员组成应包括胃肠外科、肿瘤内科、消化内科、肝脏外科、放疗科、病理科、影像科、介入科医生及护士等,甚至需要诸如心理学家、物理治疗和语言治疗专家等的参与。通过MDT会议,对相关临床信息的联合分析解读比单纯阅读个别会诊意见更有效率、更有实用性,作出的临床诊疗决策更合理,以达到尽可能使患者获得最佳的综合治疗。
Ⅳ期胃癌以解救治疗为基本目的,手术是解决合并症的手段,对于原发灶能完全切除(R0)的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,疗效可能较好,可采取相对积极的手术干预,但缺乏大样本的随机对照研究。胃癌的化疗尚无统一的金标准,疗效尚难满意,其中几种推荐方案有效率在25%~40%。
MDT模式在胃癌治疗中的应用,将改变过去“谁首诊、谁治疗”的肿瘤治疗模式,使胃癌的分期更加准确,治疗更加规范,临床医生做出的临床决策更加合理,以期达到延长肿瘤患者生存时间、提高患者生活质量的目的。
(江苏省人民医院 南京医科大学第一附属医院胃肠外科 徐泽宽 杨力 徐皓)


评论